Американські дослідники вперше пересадили в яєчко власні незрілі стовбурові клітини зародкової лінії пацієнта, забрані в дитинстві перед хіміотерапією, яка зробила його стерильним. Чи почався у нього вироблення сперматозоїдів, поки неясно. Опис методики доступний на medRXiv.org, історію пацієнта розповіло інформагентство AP.
Завдяки сучасній медицині до 85 відсотків дітей із онкозахворюваннями доживають до дорослого віку без рецидивів. При цьому приблизно кожен третій з них залишається безплідним в результаті хіміотерапії — до неї чутливі стовбурові клітини зародкової лінії, що активно діляться, які дають початок гаметам (сперматозоїдам і яйцеклітинам. Щоб дати можливість онкологічним пацієнтам мати потомство в майбутньому, в даний час пропонують кріоконсервацію. статевого дозрівання вони виробляються.
Лабораторія Кайла Оруіга (Kyle Orwig) у Піттсбурзькому університеті протягом багатьох років займається розробкою технології кріоконсервації та подальшої реплантації стовбурових клітин зародкової лінії (гаметогоній). Отримавши позитивні результати в експериментах на мавпах, дослідники почали консервацію стовбурових клітин, забраних шляхом пункційної біопсії у препубертатних дітей з онкозахворюваннями до початку хіміотерапії. З 2011 року лабораторія як клінічні випробування зберегла очищені культури таких клітин, отримані приблизно у тисячі хлопчиків.
Одним з них став Джайвен Сюй (Jaiwen Hsu), якому в 11-річному віці поставили діагноз раку кістки та почали готувати до хіміотерапії. Батьки звернулися до медичного центру Піттсбурзького університету та включили його до програми кріоконсервації стовбурових клітин. Більше 10 років він першим із пацієнтів зі збереженими клітинами звернувся за їх пересадкою - спермограма виявила у нього передбачувану азооспермію (відсутність живих сперматозоїдів в еякуляті). Сім'ю він заводити на той момент не збирався, але хотів дізнатися, чи експеримент буде успішним.
У 2023 році в рамках окремих клінічних випробувань Оруіг з колегами провів аутологічну трансплантацію суспензії клітин яєчка пацієнта, які містять сперматогонію. Для цього дослідники скористалися розробленою ними і випробуваною на тваринах технологією, яка полягає в тому, що під контролем УЗД через основу мошонки вводять голку в мережу яєчка (rete testis, галлерову мережу) - вона з'єднана з усіма насіннєвими канальцями, де відбувається утворення сперматозоїдів - і за допомогою цієї голки.
Процедура пройшла без ускладнень, після неї на УЗД тканина яєчка мала звичайну структуру. Рівні тестостерону, фолікулостимулюючого та лютеїнізуючого гормонів у пацієнта були нормальними, проте інгібіну Б (маркера сперматогенезу) – низьким. Спермограм через рік після пересадки продовжувала показувати азооспермію. Оруїг вважає, що робити висновки поки що рано — в експериментах на мавпах сперматозоїди після подібної процедури вдавалося отримати лише у невеликих кількостях пункційно, але їх успішно використовували для зачаття методом екстракорпорального запліднення. Сюй, якому зараз 26 років, зазначив, що незалежно від результатів, задоволений участю у розробці технології та вдячний батькам, які включили його до цієї програми.
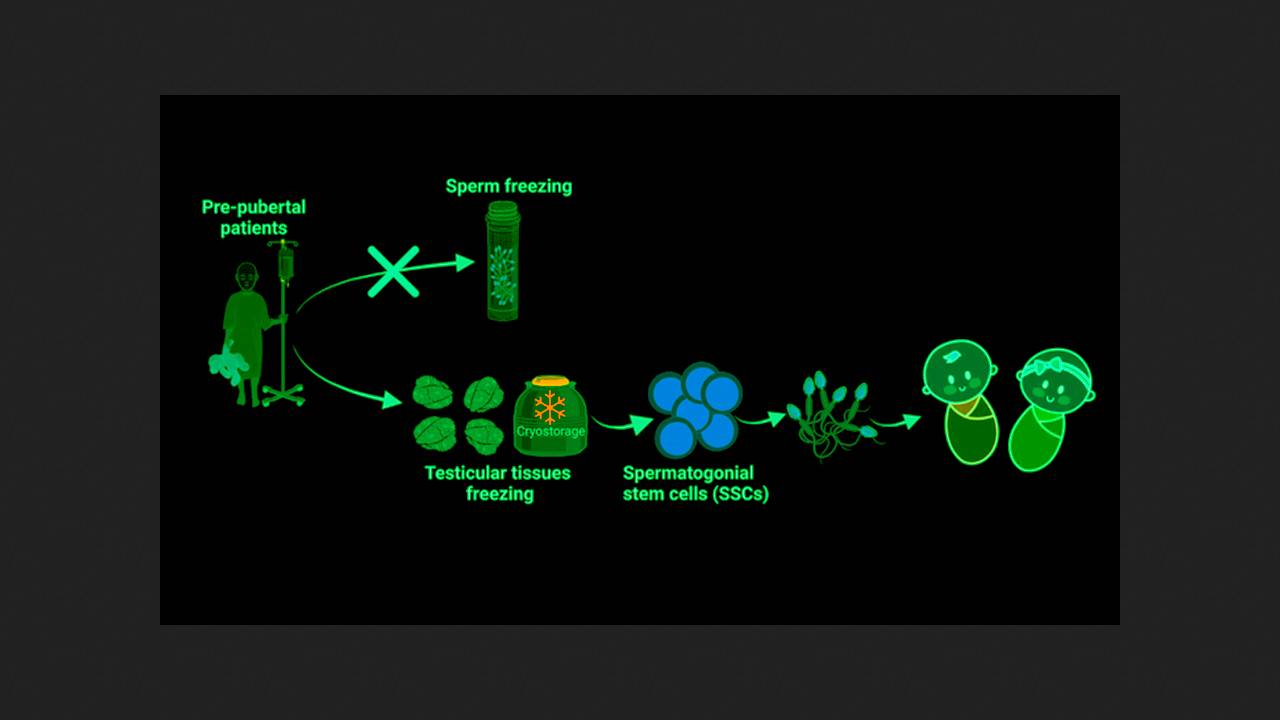
Паралельно зі збереженням стовбурових клітин зародкової лінії ведуться експерименти з кріоконсервації цілісних фрагментів тканини яєчка. У січні 2025 року Еллен Госсенс (Ellen Goossens) із колегами з Брюссельського вільного університету вперше імплантували пацієнтові такий фрагмент власної тканини. Він був забраний перед хіміотерапією у 10-річному віці та зберігався 16 років. Результати цього експерименту поки що також оцінювати зарано.