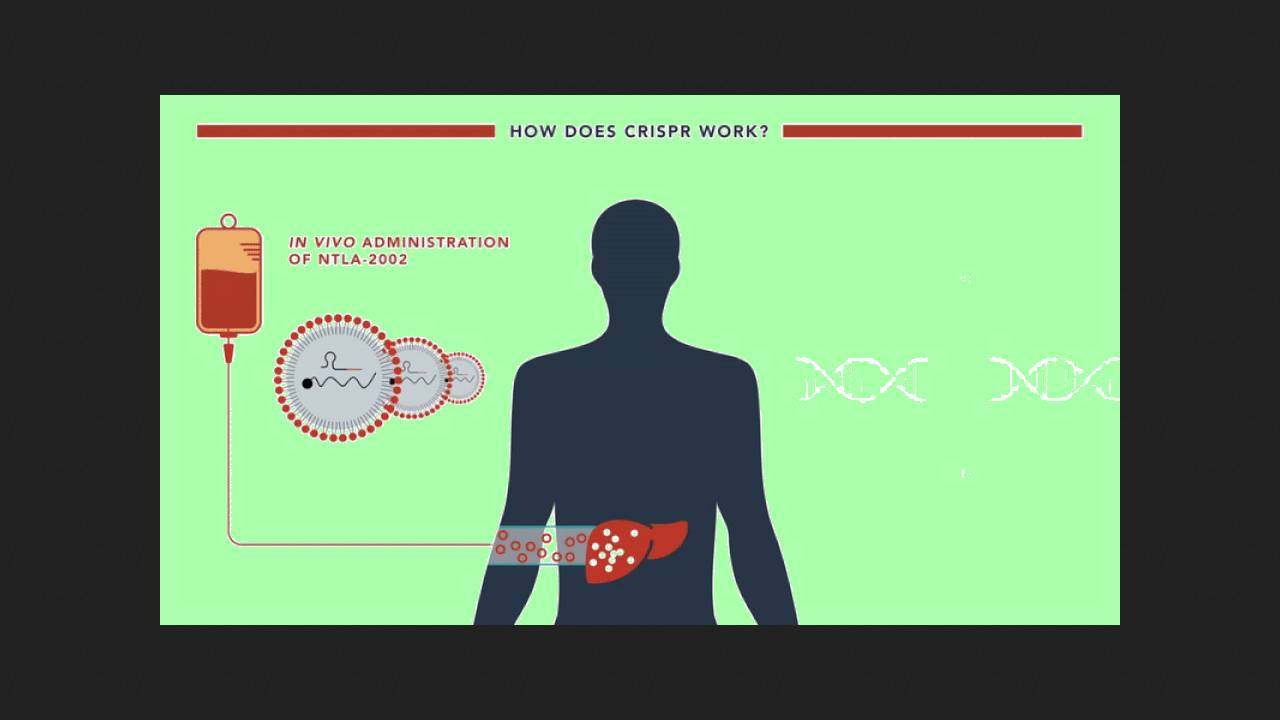
Дэнни Кон (Danny Cohn) из Амстердамского университета с коллегами из шести стран сообщили об успехе второй фазы клинических испытаний in vivo CRISPR-терапии наследственного ангионевротического отека. Экспериментальный препарат NTLA-2002 содержит упакованные в липидные наночастицы компоненты системы CRISPR/Cas9, которые при введении в организм выключают ген KLKB1, связанный с развитием заболевания (о механизме его действия и дизайне испытаний мы подробно писали ранее). Однократное введение должно обеспечивать пожизненный эффект. Во второй фазе испытаний 10 пациентам ввели 25 миллиграмм препарата, 11 пациентам — 50 миллиграмм и шести — плацебо. Результаты опубликованы в The New England Journal of Medicine.
По сравнению с плацебо в течение первых 16 недель частота приступов заболевания снижалась в среднем на 75 процентов при дозе 25 миллиграмм и на 77 процентов при дозе 50 миллиграмм; плазменный уровень калликреина по сравнению с исходным уровнем снижался на 55 и 86 процентов. При этом после введения этих доз активного препарата за период наблюдения соответственно у 40 и 73 процентов пациентов приступов не было вообще без какой-либо дополнительной терапии. Из наиболее частых побочных эффектов NTLA-2002 были зарегистрированы головная боль, повышенная утомляемость и назофарингит.