Хіміки з Німеччини навчилися вводити аніліни в реакцію крос-поєднання із бороновими кислотами. При цьому аніліни проміжно перетворювалися на діазонієві солі, які окислювально приєднувалися до паладієвого каталізатора. Дослідження опубліковано в Angewandte Chemie International Edition.
У класичному крос-поєднанні Судзукі боронова кислота і арилгалогенид реагують з утворенням зв'язку вуглець-вуглець у присутності паладієвого каталізатора. Замість арилгалогенідів у цю реакцію можна вводити аніліни, але для цього спочатку їх треба перетворювати на нестійкі та іноді вибухові діазонієві солі.
Щоб подолати цю проблему, хіміки під керівництвом Тобіаса Ріттера (Tobias Ritter) з Інституту дослідження вугілля Товариства Макса Планка вирішили застосувати нещодавно розроблений метод генерації діазонієвих солей з анілінів за допомогою нітратів. Раніше вони використовували цей метод для отримання ароматичних галогенпохідних з анілінів, і він виявився безпечнішим від класичного діазотування, тому що діазонієві солі не накопичувалося в реакційній суміші.
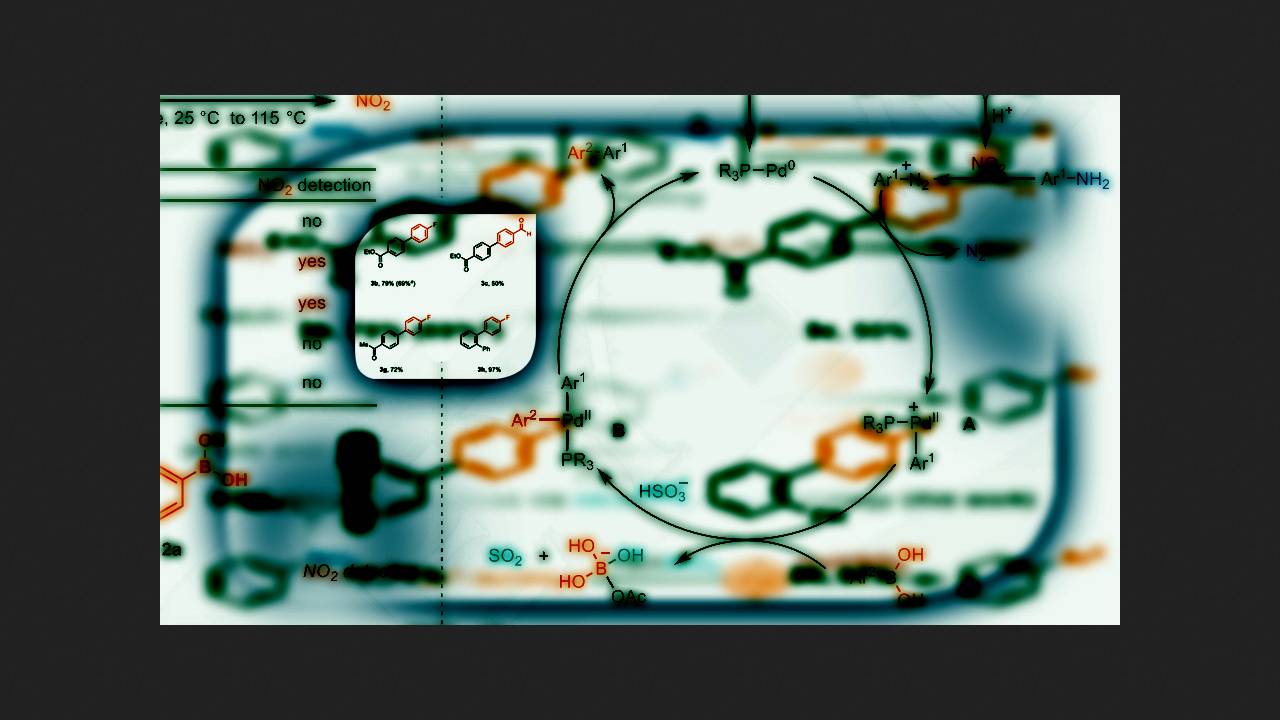
З тих же міркувань хіміки вирішили застосувати цей метод для реакції Судзукі з анілінами. Спочатку вони змішували 4-фторборонову кислоту та 4-метиланілін у присутності різних паладієвих каталізаторів, нітрату трет-бутиламонію та інших добавок. В результаті виявилося, що реакція протікає з виходом 69 відсотків, якщо як відновник використовувати гідросульфіт натрію NaHSO3. У своїй попередній роботі вчені використовували тіосульфат натрію Na2S2O3, але, як вони припускають, він занадто міцно зв'язується з каталізатором паладієвим, і реакція Судзукі в його присутності практично не йде.
Підібрані умови реакції хіміки протестували на різних анілінах та боронових кислотах. Виявилося, що їхні умови дозволяють використовувати не лише аніліни, а й аміногетероцикли. Крім того, за рахунок швидкого окислювального приєднання діазосполук, реакція йшла селективно навіть у присутності ароматичних бромпохідних. Головним недоліком цієї реакції, як зазначають автори статті, є низькі виходи продуктів при використанні боронових кислот з донорними заступниками в ароматичному кільці.
Таким чином, хіміки розробили загальний метод синтезу біарильних похідних з анілінів та боронових кислот. При цьому для генерації діазосполук вони використовували безпечніший нітратний метод, а більшість продуктів вийшли з виходами від 40 відсотків.
Нещодавно ми розповідали про те, як вчені використовували каталізатор на основі заліза, а не паладію, для проведення реакції Судзукі.