Американские исследователи разработали фармакологически активный гидрогель для профилактики послеоперационного спайкообразования. В экспериментах на свиньях он эффективно предотвращал развитие спаек после вмешательств на кишечнике, не нарушая заживление и без системной токсичности. Отчет о работе опубликован в журнале Science Translational Medicine.
Спайки образуются после 50–90 процентов операций на брюшной полости, служат основной причиной кишечной непроходимости, могут вызывать хронические боли и бесплодие, а также осложнять последующие хирургические вмешательства. Помимо дискомфорта и ухудшения качества жизни они создают дополнительную нагрузку на систему здравоохранения и приводят к большим финансовым затратам. Способов профилактики и лечения спаек с подтвержденной эффективностью в настоящее время нет, во многом из-за недостаточного понимания механизмов их образования и патогенеза спаечной болезни.
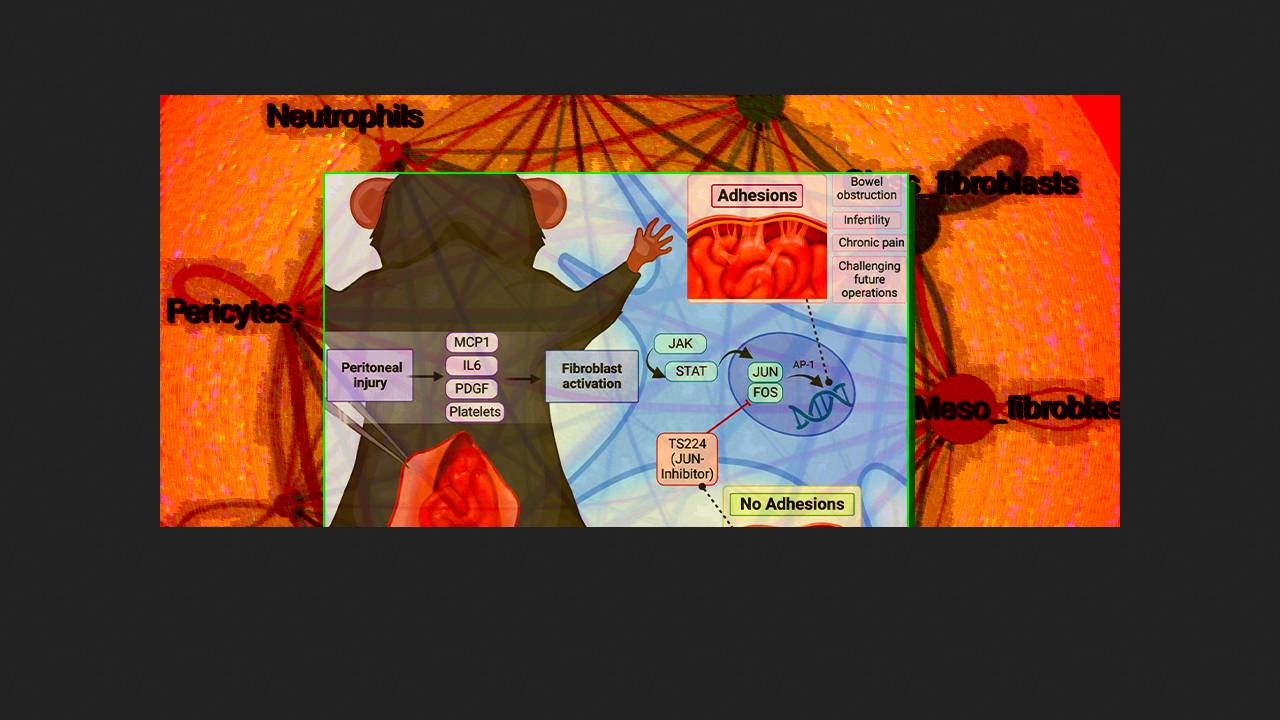
В 2020 году группа исследователей из Стэнфордского университета под руководством Майкла Лонгейкера (Michael Longaker) представила результаты фундаментального анализа спаечных тканей мыши и человека. По их данным, спайки образуются преимущественно из висцеральной брюшины в результате поликлональной пролиферации тканевых фибробластов, которые синтезируют рубцовую ткань, фиксирующую внутрибрюшные структуры и иммобилизующую кишечник. Основным регулятором этого процесса (адгезиогенеза) служит фактор транскрипции Jun, который вместе с белком Fos формирует комплекс AP-1 и запускает процесс пролиферации и синтеза внеклеточного матрикса. Низкомолекулярный ингибитор комплекса AP-1 T-5224 в эксперименте на мышах подавлял послеоперационную экспрессию Jun и ограничивал образование спаек.
Чтобы транслировать эти данные в клиническую практику, в новой работе Лонгейкер с коллегами поместили T-5224 в гидрогель гидроксипропилметилцеллюлозы с модифицированными гидрофобными боковыми цепями и сшили их биосовместимыми мицеллами детергента твина. Барьерные функции этого материала проявляют синергию с фармакологическим действием T-5224, а консистенция позволяет наносить на брюшину в месте операции с помощью шприца или спрея. Эксперименты подтвердили, что гидрогель обладает оптимальными реологическими свойствами и при миллимолярной концентрации активного препарата устойчиво высвобождает его в течение 14 дней — клинически критичного времени для образования спаек.
После успешных испытаний гидрогеля на мышах исследователи приступили к опытам на минипигах, устройство желудочно-кишечного тракта и развитие спаечной болезни у которых близко к человеческим. Для этого они разработали и проверили модель спайкообразования, включающую лапаротомию по средней линии, ревизию брюшной полости, резекцию тонкой кишки с ручным наложением анастомоза, скарификацию брюшины правой боковой стенки, промывание изотоническим солевым раствором и ушивание брюшной стенки. Замещение в этой модели солевого раствора на гидрогель с T-5224 приводило к значительно меньшему образованию спаек при ревизии через четыре недели как макроскопически, так и гистологически (в обоих случаях p < 0,0001), причем сформировавшиеся волокна матрикса в присутствии гидрогеля были менее зрелыми и плотными. Анализы показали, что T-5224 хорошо всасывался клетками местно, а его концентрация в крови была низкой и уменьшалась со временем. Признаков гематологической, печеночной и почечной токсичности, влияния на массу тела, а также гистологических изменений внутренних органов выявлено не было. На заживление кишечных анастомозов (в том числе при высокожировой диете) и их механические свойства, а также на регенерацию поврежденной кожи внутрибрюшинное введение гидрогеля значимо не влияло. Секвенирование отдельных клеток спаечной ткани показало, что использование активного препарата подавляло сигнальный путь Jun, причем эффекты этого были значительно более выраженными в мезотелиальных фибробластах, способствующих формированию фиброзных рубцов, чем в ремоделирующих фибробластах, предположительно отвечающих за регенерацию тканей после операции. Таким образом, гидрогель с T-5224 стойко препятствует образованию послеоперационных спаек брюшины без негативного влияния на состояние кишечного анастомоза и заживление брюшной стенки, а также без признаков системной токсичности. Учитывая, что биологические механизмы образования спаек схожи в различных областях хирургического вмешательства, препарат имеет потенциал к применению практически в любых анатомических локациях, считают авторы работы. Гидрогели различных составов находят применения в разных областях экспериментальной медицины: к примеру, их использовали для лечения инфаркта миокарда, закрытия язвы желудка, заживления ран при диабете, борьбы с раневыми инфекциями, повышения эффективности вакцин и соединения капилляров.