Amerykańscy chemicy opracowali ogólną metodę generowania naprężonych alkenów bicyklicznych, których istnienie jest zabronione przez regułę Bredta. Naukowcy uzyskali zbiór takich alkenów in situ, stosując eliminację synów, i poddali je różnym reakcjom cykloaddycji. Badanie zostało opublikowane w czasopiśmie Science.
Na początku XX wieku niemiecki chemik Julius Bredt podjął próbę syntezy kilku alkenów zawierających wiązanie podwójne przy mostkującym atomie węgla bicyklicznego szkieletu kamfory, wykorzystując różne reakcje eliminacji. Nie powstały żadne produkty, co skłoniło Bredta do postawienia hipotezy, że alkeny tego typu są zbyt niestabilne, aby można je było syntetyzować. To twierdzenie stało się znane jako reguła Bredta. Później odkryto, że niektóre alkeny naruszające tę regułę można wykryć spektroskopowo. Jednak naukowcom nie udało się ich zsyntetyzować ani poddać reakcji.
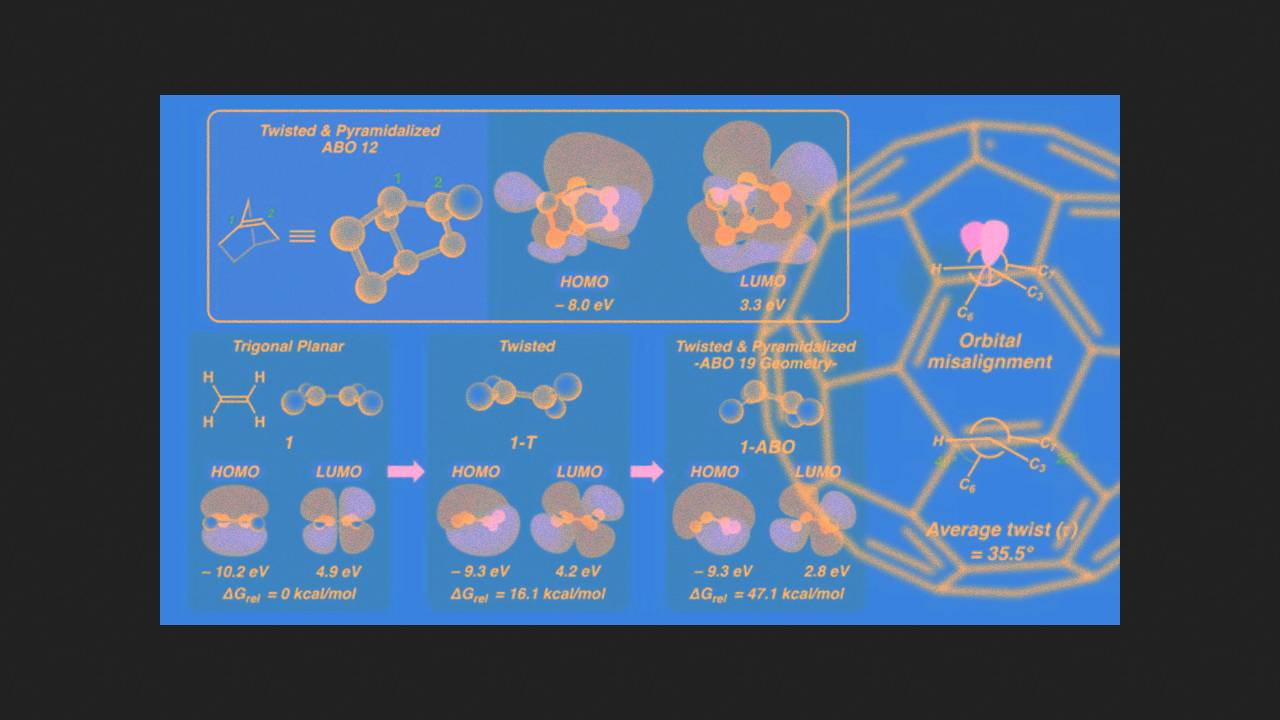
Niestabilność alkenów naruszających regułę Bredta można wytłumaczyć niefortunnym układem orbitali p atomów węgla tworzących wiązanie podwójne. Ze względu na sztywność struktury bicyklicznej, powierzchnia nakładania się tych orbitali jest bardzo mała, a wiązanie π między atomami węgla jest zbyt słabe.
Jednakże, jak wykazali chemicy pod kierownictwem Neila K. Garga z Uniwersytetu Kalifornijskiego w Los Angeles, wiązania π w takich alkenach są wystarczająco silne, aby mogły być generowane w roztworze i wykorzystywane w reakcjach cykloaddycji. Naukowcy najpierw postanowili uzyskać najprostszy alken, który narusza regułę wykluczenia Bredta – bicyklo[2.2.1]hept-1-en. W tym celu zsyntetyzowali materiał wyjściowy do reakcji eliminacji, w której grupa trimetylosililowa została przyłączona do jednego atomu węgla, a grupa trifluorometanosulfonianowa do drugiego.
Chemicy zmieszali ten materiał wyjściowy z antracenem i fluorkiem tetrabutyloamoniowym w dimetyloformamidzie w temperaturze pokojowej. Zaszła reakcja eliminacji, a powstały alken poddano reakcji Dielsa-Aldera z antracenem in situ, uzyskując produkt z wydajnością 30%. W ten sposób naukowcy potwierdzili, że alkeny naruszające zakaz mogą powstawać w roztworze.
Chemicy wykazali następnie, że ich metoda działa również z innymi bicyklicznymi materiałami wyjściowymi. Powstałe alkeny mogą ulegać nie tylko reakcji Dielsa-Aldera, ale także 1,3-dipolowej cykloaddycji. Co więcej, optycznie czyste pochodne krzemu zostały przekształcone w produkty z zachowaniem konfiguracji absolutnej.
Chemicy nauczyli się generować wysoce niestabilne alkeny, które łamią regułę Bredta. Wykorzystując opracowaną metodę, naukowcy będą mogli syntetyzować złożone związki wielopierścieniowe.
Wcześniej omówiliśmy, jak chemikom udało się po raz pierwszy uzyskać stabilny krystaliczny nitren.