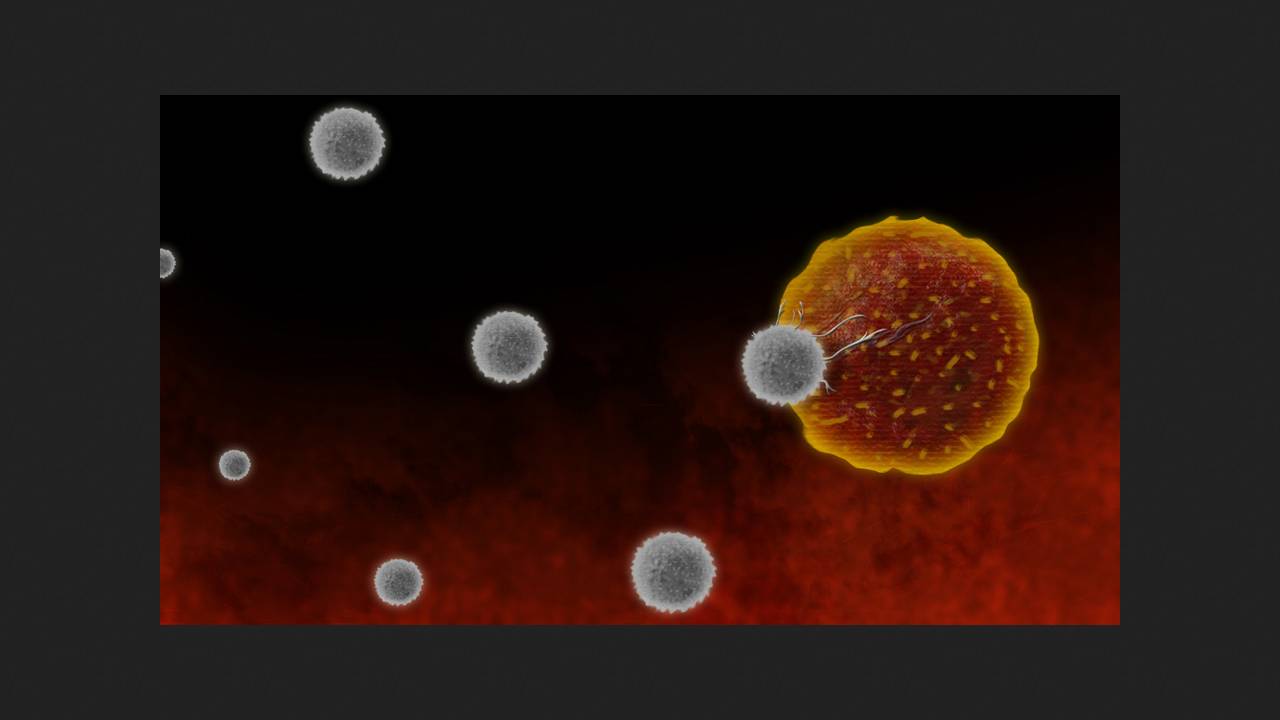
Chińscy naukowcy odnotowali sukces w badaniu klinicznym II fazy z chimerycznymi komórkami T receptorowymi antygenu CLDN18.2 w opornym raku żołądka i połączenia żołądkowo-przełykowego. Terapia ta znacząco wydłużyła życie pacjentów, zgodnie z raportem z badania opublikowanym w czasopiśmie The Lancet.
Technologia komórek T z chimerycznym receptorem antygenowym (komórki CAR-T zostały szczegółowo omówione w artykule „Chimera kontra rak”) pozwala osiągnąć długotrwałą remisję, a nawet całkowite wyleczenie u wielu pacjentów, u których inne terapie zawiodły. Ze względu na pewne ograniczenia pierwszych generacji, tylko sześć leków znalazło zastosowanie kliniczne w leczeniu hematologicznych nowotworów złośliwych komórek B i jeden w leczeniu guza litego – mięsaka maziówkowego. Terapia CAR-T w przypadku innych nowotworów znajduje się obecnie na różnych etapach badań przedklinicznych i klinicznych.
Rak żołądka i połączenia żołądkowo-przełykowego jest piątym najczęściej występującym nowotworem pod względem zapadalności i śmiertelności. Około 40% pacjentów z tymi guzami wykazuje silną ekspresję izoformy 2 klaudyny-18 (CLDN18.2). Jest to białko występujące w ścisłych połączeniach komórek nabłonkowych i jest specyficzne dla nabłonka żołądka. Ze względu na swoje położenie, ścisłe połączenia w zdrowym nabłonku są niedostępne dla działania leków biologicznych, ale CLDN18.2 w guzach może służyć jako cel terapeutyczny. Zolbetuksymab, przeciwciało monoklonalne skierowane przeciwko temu białku, jest już stosowane w leczeniu raka żołądka z ekspresją CLDN18.2, oprócz chemioterapii; wymaga regularnego podawania. Autologiczny lek na limfocyty T CAR, satricabtagene autoleucel (satric-cel, CT041), również ukierunkowany jest na ten cel i wykazał zadowalającą tolerancję oraz potencjalną skuteczność w badaniach fazy I.
Changsong Qi z Uniwersytetu Pekińskiego, wraz z kolegami i współpracownikami z CARsgen Therapeutics, przeprowadził otwarte, randomizowane badanie II fazy T041-ST-01 w 24 chińskich ośrodkach klinicznych. Do badania włączono 156 dorosłych pacjentów z HER2-ujemnym, CLDN18.2-dodatnim, opornym na leczenie, nieoperacyjnym gruczolakorakiem żołądka lub połączenia przełykowo-żołądkowego. Po limfodeplecji 104 z nich otrzymało do trzech wlewów satricelu w dawce 250 milionów komórek; pozostałych 52 pacjentów otrzymało standardową terapię niwolumabem, paklitakselem, docetakselem, irynotekanem lub rywaceranibem, według uznania lekarza.
W grupie głównej 27% uczestników otrzymało wcześniej trzy lub więcej cykli chemioterapii, a u 69% stwierdzono przerzuty do otrzewnej. W grupie kontrolnej wartości te wynosiły odpowiednio 19% i 60%. Mediana całkowitego przeżycia w grupie otrzymującej satricel wyniosła 7,92 miesiąca w porównaniu z 5,49 miesiąca w przypadku leczenia standardowego (p = 0,0416), a przeżycie bez progresji choroby wyniosło 3,25 miesiąca w porównaniu z 1,77 miesiąca (p < 0,0001). Poważne działania niepożądane zgłoszono u 99% uczestników w grupie głównej (najczęściej spadek całkowitej liczby leukocytów, limfocytów lub neutrofili) i u 63% w grupie kontrolnej. Zespół uwalniania cytokin wystąpił u 95% pacjentów po podaniu satricelu. Uzyskane wyniki pozwalają rozważyć zastosowanie satricelu jako terapii trzeciej linii w zaawansowanym, opornym na leczenie raku żołądka i połączenia żołądkowo-przełykowego HER2-ujemnym, z dodatnim wynikiem CLDN18.2. Autorzy podsumowują, że jego zastosowanie we wcześniejszych stadiach podobnych nowotworów wymaga dalszych badań. Wcześniej amerykańscy naukowcy przedstawili wyniki pilotażowego badania z zastosowaniem limfocytów CAR-T nowej generacji w nawrotowym glejaku wielopostaciowym, w którym uczestniczyło trzech pacjentów. Guzy szybko się zmniejszyły u wszystkich uczestników, ale u dwóch z nich nastąpił nawrót.