Amerykańscy chemicy otrzymali N-heterocykliczny karben, który był stabilny w roztworze wodnym. Nie ulegał protonowaniu przez wodę i nie reagował z nukleofilami ze względu na duże podstawniki karboranowe. Badanie zostało opublikowane w czasopiśmie Science Advances.
Karbeny to związki organiczne z dwuwartościowym atomem węgla w swojej strukturze. Ten atom węgla zazwyczaj ma wolną parę elektronową i wolny orbital, co sprawia, że karbeny są wysoce reaktywne wobec nukleofilów i elektrofili. N-heterocykliczne karbeny są bardziej stabilne niż inne ze względu na efekty elektronowe dwóch atomów azotu znajdujących się w pobliżu centrum karbenowego. Jednak nawet one szybko rozkładają się w powietrzu.
Chemicy pod kierownictwem Vincenta Lavallo z Uniwersytetu Kalifornijskiego w Riverside niedawno wykazali, że N-heterocykliczne karbeny mogą być stabilne nie tylko w powietrzu, ale nawet w roztworze wodnym.
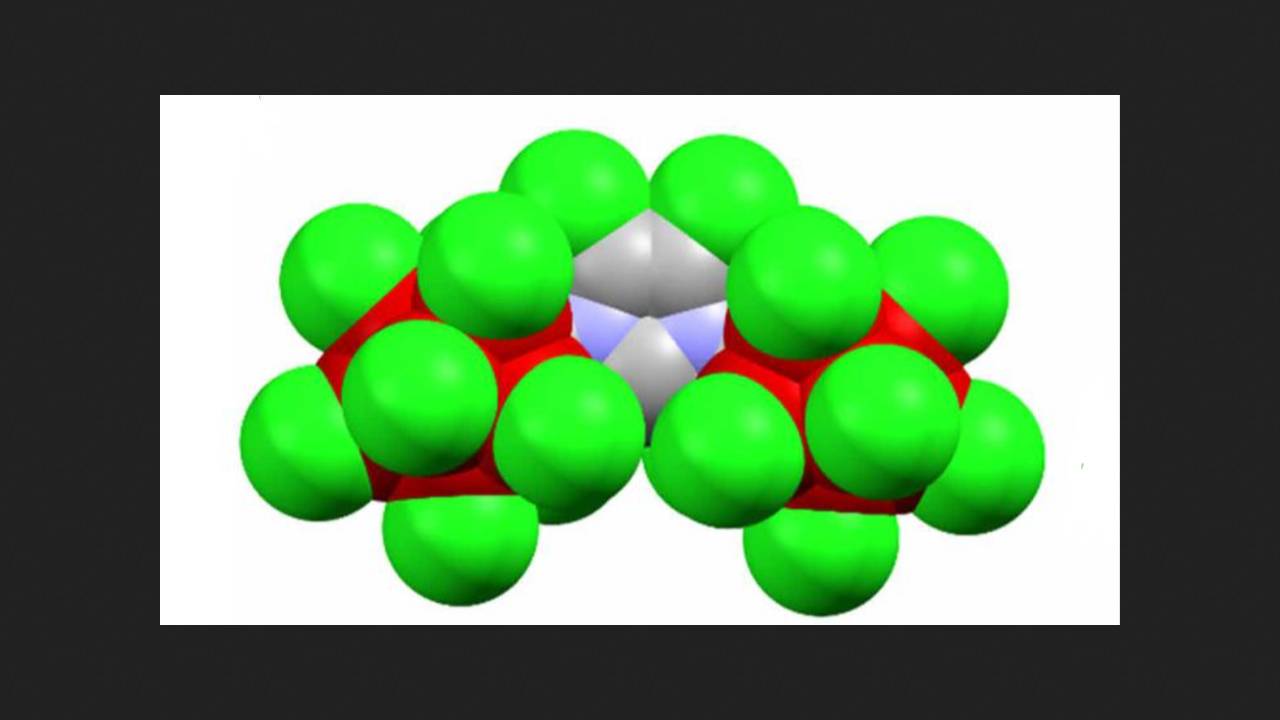
Aby uzyskać ten karben, naukowcy wprowadzili dwa duże podstawniki klastrowe (karboran) do cząsteczki prekursora N-heterocyklicznego karbenu. Podstawniki te zawierały dziewięć atomów boru i jeden atom węgla. Każdy atom boru tworzył wiązanie z innymi atomami boru, a pojedynczy atom węgla w klastrze łączył się z fragmentem karbenu. Następnie, aby zwiększyć stabilność powstałego karbenu, chemicy chlorowali te podstawniki. Teraz każdy atom boru był połączony z atomem chloru.
Chemicy zmieszali powstały chlorowany prekursor z heksametylodisilazydkiem litu, silną zasadą. W rezultacie powstał N-heterocykliczny karben. Naukowcy scharakteryzowali go za pomocą spektroskopii NMR i analizy dyfrakcji rentgenowskiej. Podczas pracy zauważyli, że jeśli luźno zamknięta ampułka NMR zawierająca roztwór karbenu była wystawiona na działanie powietrza, jej widmo NMR pozostawało niezmienione – to znaczy, że karben nie ulegał rozkładowi. Następnie do roztworu karbenu w tetrahydrofuranie dodali wodę destylowaną. Ku ich zaskoczeniu, nawet po dodaniu wody widmo NMR pozostało niezmienione. W ten sposób odkryli, że powstały karben był stabilny w roztworze wodnym.
Naukowcy wykazali następnie, że ich karben jest nie tylko stabilny w wodzie, ale można go również uzyskać w roztworze wodnym. Zmieszali prekursor karbenu i wodorotlenek litu w mieszaninie wody i tetrahydrofuranu, uzyskując czysty karben bez oznak rozkładu.
W ten sposób chemicy otrzymali pierwszy karben stabilny w wodzie. Co więcej, nie reagował on nie tylko z wodą, ale również z kompleksami różnych metali przejściowych, heterokumulenów i selenu pierwiastkowego. Autorzy artykułu sugerują, że niska reaktywność powstałego karbenu wynika z obecności podstawników elektronoakceptorowych i dużych podstawników karboranowych, które „chronią” karben przed innymi cząsteczkami.
Wcześniej omawialiśmy, jak chemikom udało się uzyskać po raz pierwszy krystaliczny nitren, który był stabilny w temperaturze pokojowej.