Brytyjscy chemicy odkryli, że kompleksy żelaza z N-heterocyklicznymi karbenami mogą katalizować reakcję sprzęgania Suzuki. Substratami były estry aromatycznego kwasu boronowego i chlorki arylu, a reakcja doprowadziła do powstania podstawionych biaryli. Badanie zostało opublikowane w czasopiśmie Nature Synthesis.
Reakcja Suzuki tworzy wiązanie węgiel-węgiel między dwiema cząsteczkami organicznymi – kwasem boronowym i halogenkiem. Sprzęganie krzyżowe jest katalizowane przez różne kompleksy palladu(0) z fosfinami, N-heterocyklicznymi karbenami i innymi ligandami. W 2010 roku japoński chemik Akira Suzuki otrzymał Nagrodę Nobla za odkrycie tej reakcji.
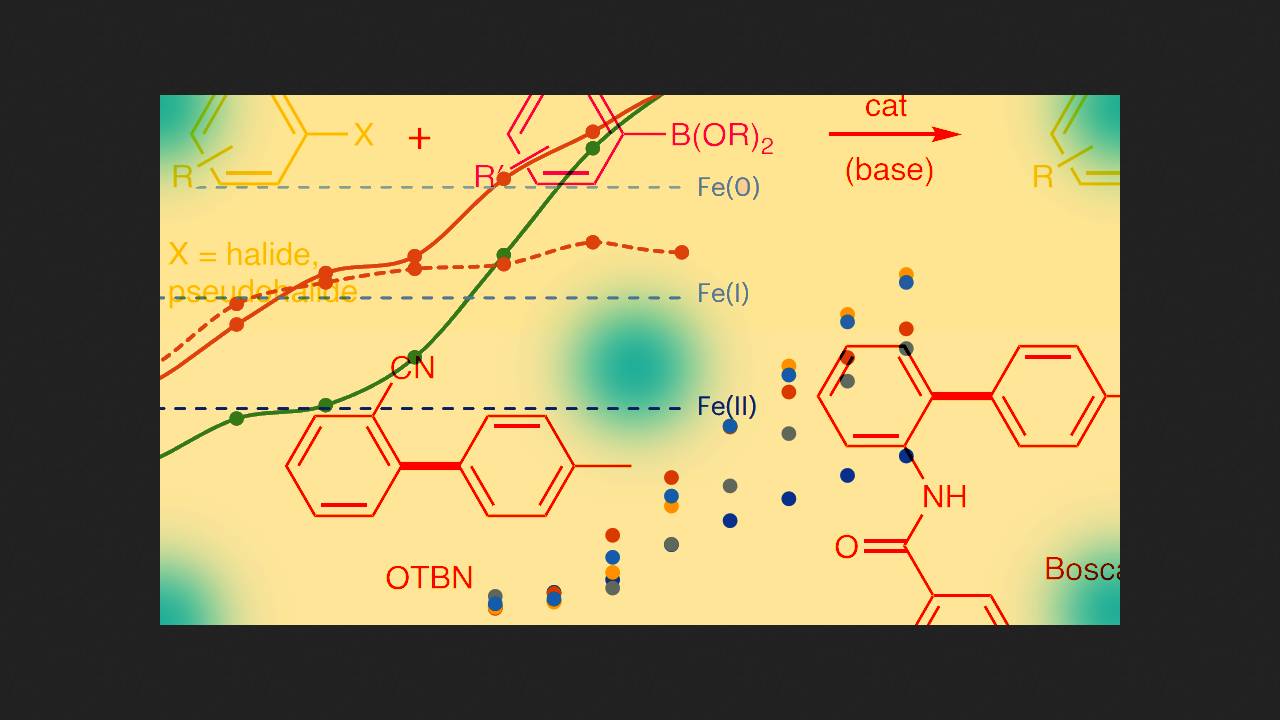
Kilka lat temu chemicy pod kierownictwem Robina B. Bedforda z Uniwersytetu w Bristolu postanowili zbadać, czy reakcję Suzuki można przeprowadzić z użyciem tańszych katalizatorów na bazie żelaza. W 2018 roku odkryli, że jest to możliwe: w obecności kompleksu karbenowo-żelazowego halogenki arylu reagowały z estrami kwasu boronowego, tworząc produkt reakcji krzyżowego sprzęgania. Jednak w reakcji uczestniczyły tylko halogenki arylu zawierające grupę kierującą sąsiadującą z halogenem.
Niedawno ci sami naukowcy odkryli, że przy starannym doborze warunków reakcji, grupa kierująca jest zbędna. Chemicy przeprowadzili reakcję w następujący sposób: zmieszali chlorek arylu, ester kwasu boronowego, bromek magnezu, bromek metylomagnezu, bromek żelaza (+3) oraz źródło ligandu karbenowego w mieszaninie dioksanu i 2-metylotetrahydrofuranu. Następnie naukowcy ogrzewali mieszaninę przez kilka godzin w temperaturze 100 stopni Celsjusza, uzyskując produkt reakcji sprzęgania krzyżowego. Jak zauważają chemicy, w większości eksperymentów jako produkt uboczny powstawał homosprzęgający produkt cząsteczek estru boronowego, który należało rozdzielić chromatograficznie.
Naukowcy wykazali ponadto, że ich reakcja działała z różnymi pochodnymi boru i chlorkami arylu, a wydajność konwersji w niektórych przypadkach sięgała 90 procent. Jeśli jednak jeden z materiałów wyjściowych zawierał grupę karbonylową lub niepodstawioną grupę aminową, pożądany produkt nie powstawał.
Chemicy odkryli zatem nową metodę przeprowadzania reakcji Suzuki z wykorzystaniem katalizatora żelazowego. Naukowcy nie ustalili jeszcze, który kompleks działa jako substancja katalitycznie aktywna. Stawiają jednak hipotezę, że w pierwszym etapie reakcji żelazo jest redukowane do +1 stopnia utlenienia, a następnie utleniająco przyłącza chlorek arylu.
Wcześniej omawialiśmy, jak chemicy nauczyli się wytwarzać diaryloaminy, stosując modyfikację reakcji Suzuki.